Tiempo de lectura aprox: 4 minutos, 52 segundos
MSD anunció este 9 de noviembre 2015 que el compromiso de la compañía con el VIH y SIDA, que empezó con un programa de investigación y desarrollo a mediados de la década de los 80 durante los primeros años de la epidemia, ahora entra en su cuarta década [1], [2]. Para conmemorar los 30 años de compromiso de MSD en esta área, la compañía está lanzando un nuevo esfuerzo, «Comprometido Positivamente«. La campaña destaca las contribuciones de la compañía, incluyendo el desarrollo de terapias innovadores para tratar las necesidades médicas insatisfechas de las personas infectadas con VIH-1 [1], [3].
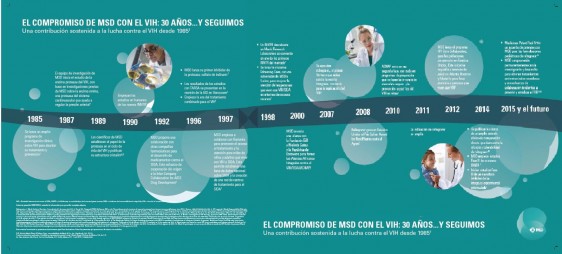
Legado de Compromiso
- A mediados de la década de los 80, poco después de que la comunidad de salud pública acuñara por primera vez el término «SIDA» para describir esta epidemia emergente, MSD comenzó su investigación sobre el VIH/SIDA [1], [2]. Los investigadores de MSD fueron los primeros en describir la estructura química de la enzima proteasa, y publicaron de inmediato los hallazgos para alentar otros esfuerzos de investigación [4]. Posteriormente los investigadores de MSD desarrollaron el sulfato de indinavir, un inhibidor de la proteasa del VIH, el cual fue aprobado en 1996 por la Agencia Europea de Medicamentos y la Agencia de Alimentos y Medicamentos (FDA por sus siglas en inglés) de Estados Unidos [1], [5], [6]. En ese entonces, la aprobación del sulfato de indinavir fue la aprobación más rápida en la historia de la FDA [7].
- En 1997, el estudio clínico de MSD con el sulfato de indinavir fue el primero en mostrar que una combinación de medicamentos antirretrovirales podía proporcionar una supresión prolongada del ARN del VIH [8].
- En 1999, MSD introdujo efavirenz, un inhibidor no nucleósido de la transcriptasa reversa (INNTR), que fue desarrollado por MSD y DuPont Pharmaceuticals [1], [9], [10]. MSD conservó los derechos para comercializarlo en mercados seleccionados fuera de Estados Unidos [10]. Actualmente es uno de los tratamientos antirretrovirales más comúnmente prescritos en el mundo [11], [12].
- A principios de 1990, MSD fue el primero en demostrar que la inhibición de la enzima integrasa del VIH-1–que se necesita para la replicación del VIH–fue posible y que al inhibir la proteína integrasa se redujo la replicación y diseminación del virus [13]. Este avance en la investigación condujo al desarrollo de raltegravir [1].
En 2007, la aprobación de raltegravir introdujo una nueva clase de tratamientos, los inhibidores de la transferencia de una cadena de la integrasa del VIH-1 [1[.
En la actualidad, los esfuerzos de investigación de MSD incluyen programas para desarrollar tratamientos y tecnología novedosos para el tratamiento y prevención del VIH, y colaboraciones sobre enfoques para abordar la latencia y la erradicación del VIH [1].
Asimismo, desde mediados de la década de los 80 poco después de que se identificó el virus del VIH, MSD se dedicó a uno de los programas más grandes de investigación de la vacuna contra el VIH, que culminó en un estudio a gran escala que ilustró la dificultad del desarrollo exitoso de una vacuna contra el VIH [1]. En la actualidad, los esfuerzos de investigación de MSD incluyen programas para desarrollar tratamientos y tecnologías de prevención novedosos contra el VIH, y colaboraciones sobre enfoques para abordar la latencia y la erradicación del VIH [1].
La investigación es sólo una parte de nuestra estrategia integral para hacer frente a las necesidades insatisfechas en el VIH. MSD también ha buscado aumentar el acceso a nuestros medicamentos para el VIH, sobre todo en entornos de recursos limitados [1], [3].
“Los tratamientos eficaces para la infección por VIH-1 eran una esperanza lejana en la década de los 80, pero el descubrimiento científico de colaboración y el apoyo eficaz lo han hecho posible hoy«, dijo Julie Gerberding, Vicepresidenta Ejecutiva, Comunicaciones Estratégicas, Políticas Públicas Globales en MSD [14], “Estoy orgullosa de que MSD está comprometido con sostener nuestras contribuciones para el tratamiento de esta infección en todo el mundo” [1].
Afrontar el desafío del VIH/SIDA a través de la colaboración
Desde la concepción de su programa de investigación sobre el VIH/SIDA hace 30 años, MSD ha reconocido la repercusión mundial del VIH/SIDA en los países en desarrollo, en donde los factores económicos, sociales y políticos impiden el acceso a la educación, la atención y el tratamiento [1], [3]. La Fundación Merck, una fundación privada basada en Kenilworth, Nueva Jersey, Estados Unidos, se ha asociado con los gobiernos, las organizaciones no gubernamentales y otras partes interesadas, aportando más de $122 millones de dólares en los últimos 15 años para apoyar los programas de intervención, fortalecer la capacidad de salud y mejorar el acceso al tratamiento. A parte de eso, MSD ha brindado estrategias de acceso, como precios diferenciales y licencias de fabricación de forma voluntaria, para mejorar el acceso al tratamiento en estas comunidades [1], [3], [15].
Este 2015, MSD se asoció con el Medicines Patent Pool para proporcionar acceso a raltegravir para bebés y niños a partir de cuatro semanas a menores de 12 años de edad en los países en desarrollo de bajos y medianos ingresos [16], [17].
El compromiso en marcha continúa
Al respecto de su compromiso MSD expresó que «la dedicación inquebrantable de MSD para pacientes que viven con el VIH continúa, y es una parte de nuestro gran compromiso sostenido para el desarrollo de medicamentos y vacunas para combatir una amplia gama de enfermedades infecciosas [18]«.
Referencias
- Merck.com. HIV Research. http://www.merckresponsibility.com/access-to-health/infectious-diseases/hiv-aids/hiv-research/. Consultado en junio 2015.
- The AIDS Institute. Where Did HIV Come From? http://www.theaidsinstitute.org/education/aids-101/where-did-hiv-come-0. Consultado en junio 2015.
- Merck.com. HIV/AIDS Availability and Affordability. http://www.merckresponsibility.com/access-to-health/infectious-diseases/hiv-aids/availability-affordability/. Consultado en junio 2015.
- Merck.com. Newsroom: Merck Signs Two Deals for Novel HIV Drug Candidates and Initiates Phase II Clinical Trial of MK-1439 for HIV. http://www.merck.com/licensing/our-partnership/Merck-chimerix-partnership.html. Consultado en junio 2015.
- European Medicines Agency. Crixivan. http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/000128/human_med_000729.jsp&mid=WC0b01ac058001d124. Consultado en junio 2015.
- U.S. Food and Drug Administration. FDA Approved Drug Products: Crixivan. http://www.accessdata.fda.gov/scripts/cder/drugsatfda/index.cfm?fuseaction=Search.DrugDetails. Consultado en junio 2015.
- Philly.com. A Potent Drug For Aids Wins Swift Approval The Fda Acted In Record Time. Merck’s New Drug Has Shown An Ability To Sharply Reduce The Virus. http://articles.philly.com/1996-03-15/news/25636506_1_fastest-drug-approval-drug-indinavir-undetectable-levels. Consultado en junio 2015.
- Jon Cohen AIDS Research Collection. New Studies Show Triple-Therapy with Crixivan (R) Drops HIV to Undetectable Levels in Patients in All Stages of HIV Disease. http://quod.lib.umich.edu/c/cohenaids/5571095.0120.055?hi=0;rgn=main;view=fulltext;q1=crixivan. Consultado en junio 2015.
- European Medicines Agency. Stocrin. http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/000250/human_med_001066.jsp&mid=WC0b01ac058001d124. Consultado en junio 2015.
- U.S. National Library of Medicine and National Institute of Health. Efavirenz DuPont Pharmaceuticals Co. http://www.ncbi.nlm.nih.gov/pubmed/18465625. Consultado en junio 2015.
- Journal of Antimicrobial Chemotherapy. Secondary metabolism pathway polymorphisms and plasma efavirenz concentrations in HIV-infected adults with CYP2B6 slow metabolizer genotypes. http://jac.oxfordjournals.org/content/early/2014/04/11/jac.dku110.full.pdf. Consultado en junio 2015.
- U.S. National Library of Medicine and National Institute of Health. Efavirenz-Based Regimens in Antiretroviral-Naive HIV-Infected Patients: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. http://www.ncbi.nlm.nih.gov/pubmed/25933004. Consultado en junio 2015.
- Business Wire. Press Release: An Investigational Oral HIV Integrase Inhibitor, MK-0518, in Combination Therapy Achieved Comparable HIV RNA Reduction to Efavirenz in Combination Therapy in Treatment-Naive, HIV-Infected Patients at 24 weeks. http://www.businesswire.com/news/home/20060812005002/en/Investigational-Oral-HIV-Integrase-Inhibitor-MK-0518-Combination#.VXmxrflVikp. Consultado en junio 2015.
- PhRMA. New Medicines Yield Significant Progress against Serious Diseases. http://www.phrma.org/sites/default/files/pdf/medical_advances_final_9.4.12.pdf. Consultado en junio 2015.
- Merck.com. Merck Corporate Responsibility Report 2011. http://www.merckresponsibility.com/downloads/MRK_Report_Builder_Full_120824.pdf. Consultado en junio 2015.
- Merck.com. Newsroom: Merck Announces Collaboration with the Medicines Patent Pool to Expand Access to Pediatric Formulations of Raltegravir in Developing Countries. http://www.mercknewsroom.com/news-release/prescription-medicine-news/merck-announces-collaboration-medicines-patent-pool-expand-a. Consultado en junio 2015.
- World Health Organization. Pediatric Advocacy Toolkit. http://whqlibdoc.who.int/hq/2011/WHO_HIV_11.04_eng.pdf?ua=. Consultado en junio 2015.
- Merck.com. Resistance: Infectious Diseases. http://www.merck.com/about/featured-stories/infectious_disease.html. Consultado en junio 2015.



